
首页 > 技术文章 > 抗 TN Fα 单抗不同粒径级别蛋白聚体监测结果的比较与评价
2020-04-16

单抗稳定性研究是贯穿于整个药品研发、临床试验、药品上市及上市后研究的重要内容,是药品储存条件、有效期等的设定依据,也是对产品生产工艺、制剂处方、包装材料等的适用性进行判断的参考,同时也是产品质量标准制订的基础。 在单抗稳定性研究中,单抗分子往往会发生聚集,形成由小而大的不同粒径级别的聚体,这些聚体是产品相关杂质,具有潜在的免疫原性。
SEC-HPLC可高效、快捷地检测单抗药物的聚体含量,已广泛用于单抗等生物制品的质控分析, 但是使用这种方法往往面临需要对样品进行稀释而导致不稳定得纳米级蛋白聚集体发生解离,或者微米级的颗粒在色谱柱外或色谱柱的凝胶中被截留,无法通过该方法得到有效展示,又或者由于SEC-HPLC采用紫外检测器,分辨率有限,使聚体得不到有效分离等问题。
FlowCam®(MDI,微流数字成像法)可以反映样品中微米级颗粒的数量及粒度,并提供颗粒图像信息。通过专用软件可以帮助使用者将颗粒进行分类,轻松分辨出硅油,气泡,蛋白质聚集体,还是金属,橡胶,玻璃等脱卸物。
将两种方法合起来分析更有助于对稳定性研究中样品各粒径级别蛋白聚体真实状态的全面评估。
目的:探讨在单克隆抗体(单抗)稳定性研究中,分子排阻高效液相色谱法(size exclusion-high performance liquid chromatography,SEC-HPLC)、微流数字成像(microflow digital imaging,MDI)技术、澄清度及可见异物检查在不同粒径级别蛋白聚体监测中的交互作用。
方法:分别采用SEC-HPLC、MDI、澄清度及可见异物检查研究肿瘤坏死因子α(TNFα)靶点单抗在4℃储存6个月、37℃和6000 lx 光照条件下储存28 d后,蛋白聚体、不溶性微粒、澄清度及可见异物的不同变化。

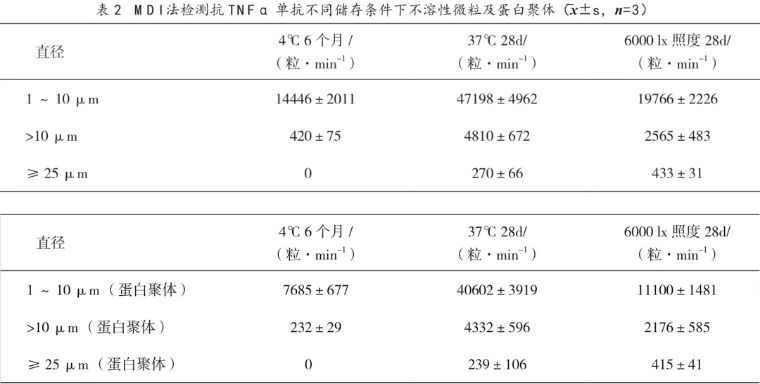
结果:SEC-HPLC结果表明,与样品在4℃储存6个月的结果相比,抗TNFα单抗的蛋白聚体含量在37℃和6000 lx照度处理28d后均增加均不明显。使用MDI技术可见,抗TNFα单抗经37℃和6000 lx照度处理28 d后,1~10 μm、10 μm以上、25 μm及以上粒径的微粒数量比在4℃储存6个月的样品有明显增多,且增多的微粒主要为蛋白聚体。通过目视法对样品的澄清度和可见异物检查发现,37℃储存和6000 lx照度处理28 d后的抗TNFα单抗澄清度低于4℃储存的样品;各储存条件下的抗TNFα单抗均未检出可见异物。

图 1 三种储存条件下抗 TN Fα 单抗的 SEC -H PLC 图谱
讨论:在单抗稳定性研究中,纳米级、微米级蛋白聚体的形成上并不具有一致性,因此,应采用多种方法对蛋白聚集情况进行表征和分析,避免单一方法的局限。
郭莎,张峰等,中国食品药品检定研究院单克隆抗体产品室 卫生部生物技术产品检定及标准化重点实验室,一种抗 TN Fα 单抗不同粒径级别蛋白聚体监测结果的比较与评价,2018,32(8):1073-1078
Fluid Imaging Technologies(FlowCam)公司成立于1999年美国缅因州斯卡伯勒市,其研发并生产的FlowCam系列仪器是将流式细胞法组合到数字成像显微镜中,基于图像分析法的流式动态成像颗粒分析仪,它使颗粒分析变得更快,更简单。具有革新意义的FlowCam系列仪器被广泛应用于研发和质量控制,应用涉及多个领域。
FlowCam® 8100作为MDI新型号已经替代文中所提到的FlowCam® VS-1。新型号为生物制药行业作出特别优化,具有以下先进性能:
小样品需求量100μL
测量范围:1~1,000μm
测样率:100% (无检测盲区)
成像系统分辨率:单色1920X1220
进样效率:50μL~5,000μL无极调速
快门速度:高可达100帧/秒
大样品浓度(@2.5μm):5,000,000颗/毫升
颗粒图像显示:显示样品所有颗粒图像
自动进样器(选配):具备加热,冷却,定轨摇床,紫外杀菌和HEPA正压过滤,大连续进样量:2X96
校准校验:使用NIST授权标准珠进行粒度和浓度检测校准校验
实验结果:30+颗粒形态参数,直方图,散点图,TIFF格式颗粒图像,所有数据均可导入PDF和Excel文件
软件合规性:满足21CFR Part11

